研究背景
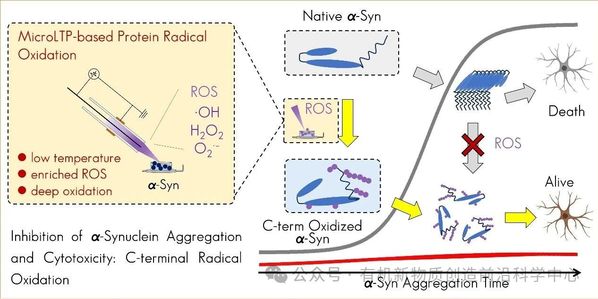
在神经退行性疾病的漫长研究征途上,帕金森病、路易体痴呆等病症如同难以攻克的“黑暗城堡”,而 α- 突触核蛋白(α-Syn)的异常聚集,正是这些城堡中释放“毒雾”的罪魁祸首。长久以来,科学界深信氧化应激是推动蛋白质错误折叠、加速疾病进程的“帮凶”,然而南开结构质谱团队的最新研究,却如同刺破迷雾的利剑,带来了颠覆性的认知。
α-Syn 是神经元突触中活跃的“通信员”,肩负着调控神经递质释放的重任。但在帕金森病等疾病侵袭下,它会“叛变”,错误折叠并聚集成淀粉样纤维,形成标志性的路易小体。这些异常聚集体不仅阻断神经元间的“通信”,还会引发氧化应激、线粒体功能障碍和神经炎症,最终将神经元推向死亡深渊。大脑因高耗氧量、富含不饱和脂肪酸且抗氧化能力较弱,犹如一座易攻难守的城池,时刻面临活性氧(ROS)的“攻城略地”,氧化应激也因此成为多种蛋白质异常聚集的关键推手。
不过近年来,科研界出现了令人困惑的现象:特定的氧化修饰似乎能抑制蛋白质聚集,这让科学家们不得不重新审视氧化应激与蛋白质错误折叠之间的关系。近日,南开大学李功玉课题组在国际顶尖学术期刊《美国化学会志》(Journal of the American Chemical Society)发表题为《C-terminal Radical Oxidation Inhibits α-Synuclein Aggregation and Cytotoxicity via an Oxidative Oligomer-disrupting Pathway》的最新研究论文,终于为这一谜题揭开一角。
论文简介
李功玉课题组凭借自主搭建的非变性氧化装置(microLTP),搭配离子淌度质谱(IM-MS)和液相色谱 - 串联质谱(LC-MS/MS)等“精密探测仪”,深入探索 α-Syn 的“隐秘角落”,发现了 C末端的高氧化修饰偏好对完整 α-Syn 结构和功能的“守护力量”。更令人惊叹的是,他们证实这种特异性氧化抑制聚集的 “超能力”,仅在蛋白质聚集前有效。一旦聚集完成,氧化便失去了“修复魔法”,无法逆转其神经毒性。这一发现彻底改写了传统认知,为神经保护策略开辟了全新赛道 —— 尽早进行氧化干预,或许能成为对抗神经退行性疾病的“新武器”。
研究亮点
这项研究是李功玉课题组在构象分辨质谱应用方法学领域的又一次重大突破。此前,团队已在短肽显著结构差异分析和大蛋白微小结构差异表征方面取得多项成果(J. Am. Chem. Soc. 2025; Chem. Sci. 2024/2023; Angew. Chem. Int. Ed. 2023; Anal. Chem. 2025/2024/2023/2022)。此次,他们成功实现了蛋白质在位点特异性层面的氧化修饰及其在结构和功能调控中的应用,为深入探究蛋白质位点特异性的调控机制奠定了坚实基础。
研究内容
研究中,团队利用微尺度低温等离子体(microLTP)装置模拟细胞病理状态下的氧化应激“战场”,结合高分辨质谱分析,如同给 α-Syn 做了一次“精密体检”。结果发现,α-Syn 的整体高氧化水平主要由 C末端的 M116、M127 和 Y133 残基“掌控”,这不仅证实了 C末端尾部更高的构象灵活性,还表明基于 LTP 的自由基氧化可作为识别 α-Syn 构象灵活区域的“结构探针”。
进一步研究如同抽丝剥茧,团队发现自由基氧化如同“精准卫士”,以剂量依赖性方式逐步抑制寡聚物及纤维的形成,却对单体蛋白的结构“秋毫无犯”。这意味着基于 C末端高效氧化介导的抑制作用,可能在初始聚集成核阶段,就阻止或破坏关键低聚物的形成。而且,单体 α-Syn 氧化的聚集抑制效果,能够显著降低其聚集产物的细胞毒性,但这种“解毒能力”在已形成纤维的氧化处理中却消失不见,充分证实了这种氧化调控的单向性。
为深入剖析结构域水平上的氧化调控对 α-Syn 功能的影响,研究人员对不同结构域的代表性短肽进行氧化调控实验。结果再次印证,C末端氧化凭借其高氧化水平,在 LTP 介导的氧化过程中,成为了“关键指挥官”,发挥着最为重要的调控作用。
这项研究不仅提出了氧化修饰在 α-Syn 聚集和相关神经毒性中作用的全新观点,更为氧化修饰介导的蛋白质结构和功能调控关系研究带来新启示。未来,该研究成果有望在多个方向“开花结果”:深入探究 α-Syn 氧化在疾病中的作用,将单一蛋白氧化调控的研究拓展至复杂疾病环境;探索神经退行性疾病中其他淀粉样蛋白是否存在类似的氧化低聚物干扰途径;开发更精细的蛋白质位点特异性氧化方法,进一步阐明易于聚集的蛋白质结构 - 功能关系。南开结构质谱团队的这一颠覆性发现,正为神经退行性疾病的研究和治疗点亮新的希望之光。

图1 基于LTP氧化装置的α-Syn的自由基氧化表征
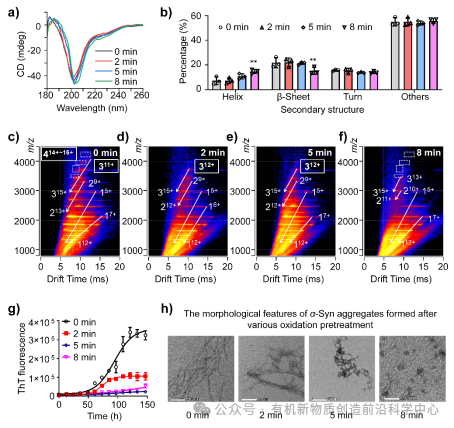
图2 自由基氧化介导的α-Syn的构象转变、寡聚体及组装抑制机制

图3 单体α-Syn(而非纤维)的自由基氧化抑制细胞毒性作用
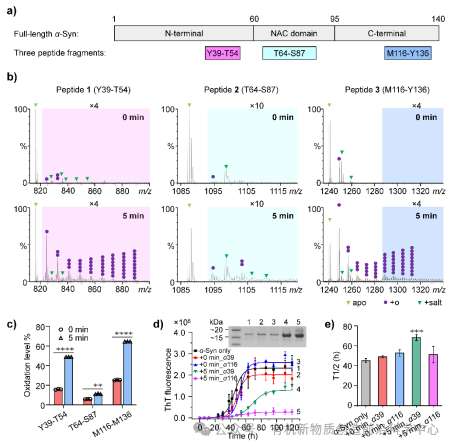
图4 结构域特异性自由基氧化验证C-末端氧化的关键作用
南开大学化学学院2023级博士研究生王晓丽为该文第一作者,李功玉研究员为本文通讯作者,南开大学有机新物质创造前沿科学中心为论文通讯单位。中国科学技术大学刘扬中教授、安徽农业大学曹开明教授、天津医科大学郑珍教授和南开大学王倩倩、刘宁老师对本项目提供了重要的技术支持。本文主要质谱数据均采集于《药物化学生物学全国重点实验室》和《天津物质绿色创造与制造海河实验室》结构质谱分析平台。本研究工作获国家重点研发计划青年科学家项目资助。
论文信息
C-terminal Radical Oxidation Inhibits α-Synuclein Aggregation and Cytotoxicity Via an Oxidative Oligomer-disrupting Pathway,Xiaoli Wang, Tingting Liang, Anran Jin, Chenao Zhang, Jiaxin Zhou, Mingrui Li, Ziyi Sun and Gongyu Li*, J. Am. Chem. Soc. 2025, xxxx. https://doi.org/10.1021/jacs.5c06792
作者简介
第一作者:王晓丽,硕士毕业于天津大学,2023年进入南开大学化学学院攻读博士学位(导师:李功玉研究员),研究课题主要聚焦蛋白质微小结构异质性的结构质谱方法开发与应用。
通讯作者:李功玉,南开大学化学学院,特聘研究员、博士生导师。国家高层次青年人才计划入选者、国家重点研发计划青年项目首席科学家。2017年博士毕业于中国科学技术大学化学系,随后在密西根大学和威斯康星大学麦迪逊分校完成博士后研究,于2021年2月加入南开大学化学学院,研究方向为蛋白结构质谱分析。




