
研究背景
胰腺导管腺癌(PDAC)是一种高度恶性的肿瘤,占胰腺癌病例的90%以上,5年生存率仅为约10%。目前的手术切除和化疗效果有限,亟需开发新型治疗策略。mRNA疗法在COVID-19疫苗中取得成功,但其在胰腺组织中的靶向递送仍面临挑战,尤其是针对胰腺导管上皮细胞(PDECs)的递送系统尚未有效建立。
研究内容
南开大学化学学院、有机新物质创造前沿科学中心熊虎研究员团队首次报道了一类新型含硫缩酮的生物可降解离子化脂质(TBILs),可高效将 mRNA 递送至胰腺及导管上皮细胞。其中,具有四个硫缩酮桥连接头的脂质分子 4A2 - B8 - PH 被确定为最优候选物,该分子具备优异的内体逃逸能力和 mRNA 释放效率。与不含硫缩酮的脂质纳米粒(LNP)不同,后者经腹腔注射后会介导 mRNA 在多个器官中广泛表达,而 4A2 - B8 - PH 脂质纳米粒可实现 mRNA 的胰腺特异性递送,靶向特异性高达 98.3%。此外,该脂质纳米粒对胰腺组织的 mRNA 递送效率显著提升,较以往的胰腺靶向脂质纳米粒基准值高出两个数量级。值得注意的是,经优化的2脂质纳米粒能够在胰腺导管上皮细胞中实现高效的 mRNA 表达,对目标细胞群的转染率达到 30.5%。更令人振奋的是,在原位胰腺导管腺癌小鼠模型中,注射包裹白细胞介素 - 12(IL - 12)mRNA 的 4A2 - B8 - PH 脂质纳米粒可实现肿瘤的完全清除,同时避免了全身性脱靶毒性。综上,该研究为推进胰腺靶向脂质纳米粒的研发奠定了基础,同时解决了向导管上皮细胞高效递送 mRNA 这一难题,为难治性胰腺疾病的治疗提供了新途径。该工作以“Thioketal-Incorporated Biodegradable Lipid Nanoparticles Deliver mRNA to Ductal Epithelial Cells for Improved Pancreatic Cancer Treatment”为题,发表在JACS期刊上,南开大学有机新物质创造前沿科学中心为论文通讯单位。
文章亮点
1. 创新性设计:开发了硫缩酮修饰的可生物降解离子化脂质(TBILs),显著提高了胰腺靶向性和mRNA递送效率。
2. 高效递送:4A2-B8-PH LNPs在胰腺组织中实现了98.3%的靶向特异性和218倍于现有基准的递送效率。
3. 细胞特异性转染:首次实现了胰腺导管上皮细胞的高效转染,为PDAC治疗提供了新的策略。
4. 免疫治疗效果显著:通过递送IL-12 mRNA,实现了原位PDAC小鼠模型的完全肿瘤消退,且无系统性毒性。
5. 临床转化潜力:为开发针对胰腺疾病的mRNA疗法提供了重要的基础。
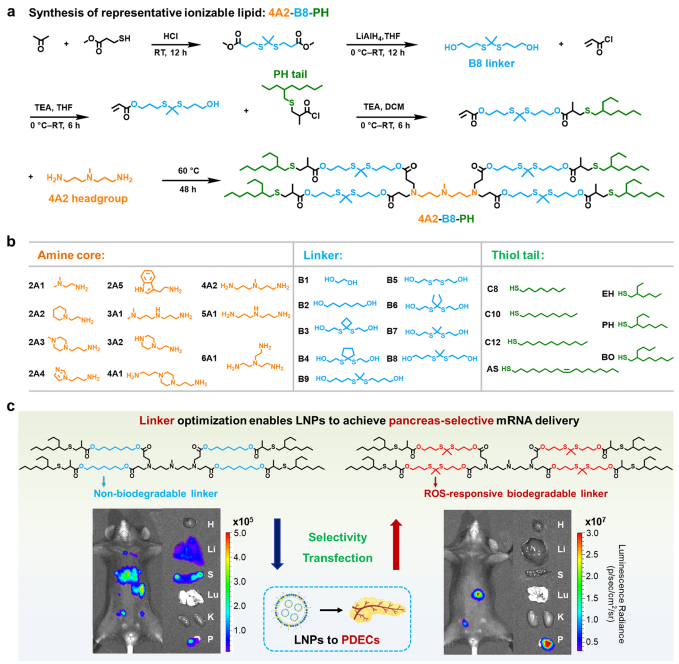
图1:展示了TBILs的模块化设计与合成路线,包括胺头基、连接基和硫醇尾的组合库,为后续筛选提供结构基础。
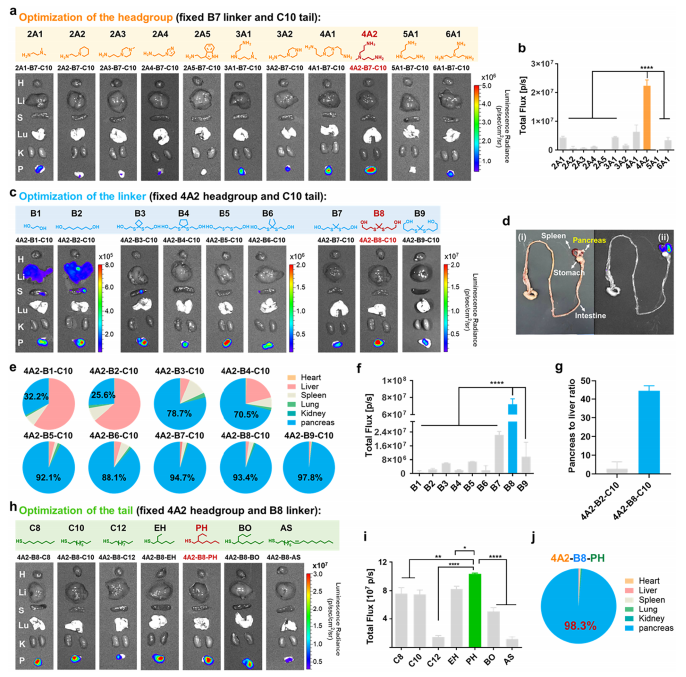
图2:通过体内外筛选系统评估不同TBILs结构对胰腺靶向性与转染效率的影响,最终确定4A2-B8-PH为最优候选。
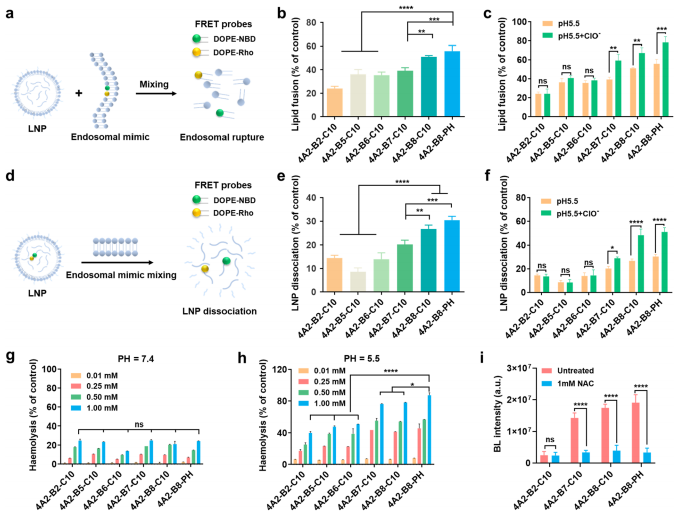
图3:利用FRET和溶血实验证明硫缩酮连接基显著增强LNPs的内体逃逸与膜融合能力,促进mRNA在肿瘤细胞中的释放。
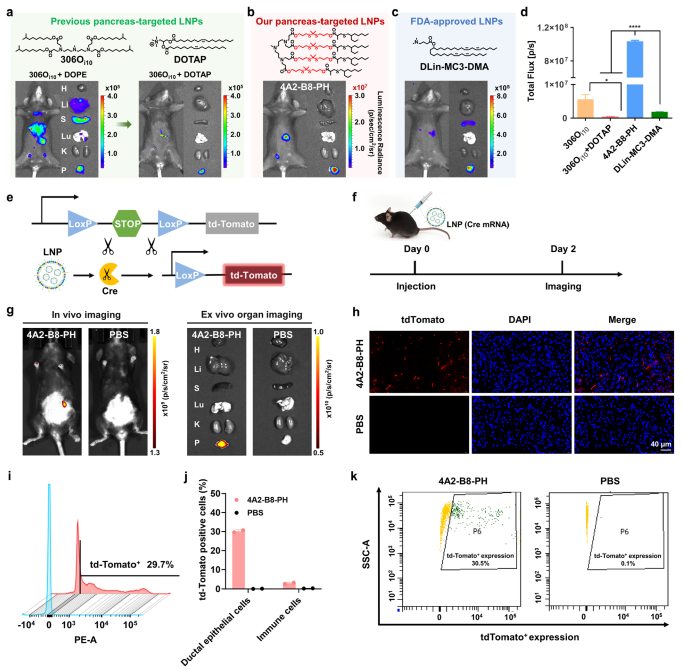
图4:比较4A2-B8-PH LNPs与现有LNPs(如306O110和MC3)的胰腺靶向效率,显示其218倍的提升及在PDECs中的高效基因编辑能力。
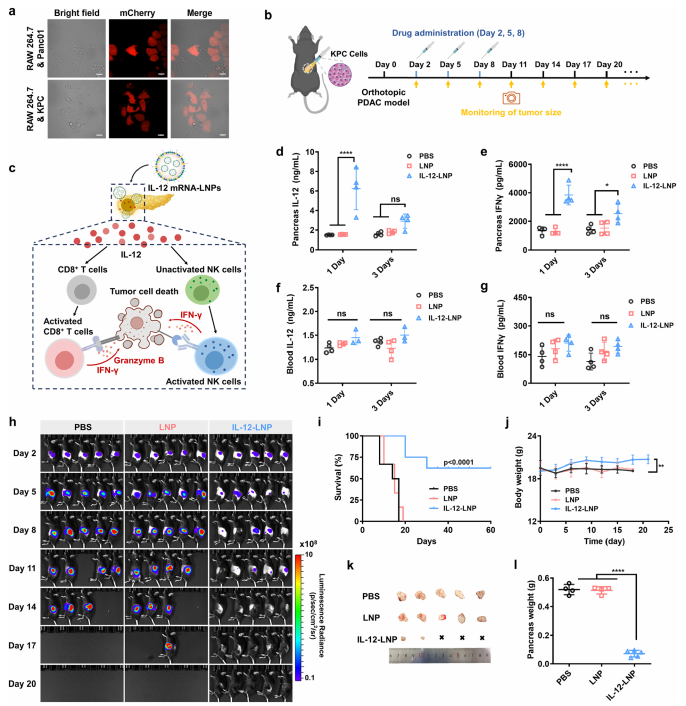
图5:在原位PDAC模型中,IL-12 mRNA-loaded 4A2-B8-PH LNPs通过重塑免疫抑制微环境,显著抑制肿瘤生长并实现完全消退,验证其治疗潜力与安全性。
总结与展望
作者成功开发了一种新型的硫缩酮修饰的可生物降解离子化脂质(TBILs),并筛选出最佳候选脂质4A2-B8-PH,用于高效的胰腺靶向mRNA递送。4A2-B8-PH脂质纳米颗粒(LNPs)在体内表现出卓越的胰腺靶向特异性(98.3%)和显著提升的mRNA递送效率,比现有基准高出218倍。此外,这些LNPs首次实现了胰腺导管上皮细胞的高效转染(30.5%),并通过递送白细胞介素-12(IL-12)mRNA在原位胰腺导管腺癌(PDAC)小鼠模型中实现了完全肿瘤消退,同时避免了系统性毒性。后续研究可从以下几个维度深入拓展:首先,可进一步探索4A2-B8-PH LNPs搭载CRISPR-Cas9 mRNA用于矫正PDAC中KRAS等关键基因突变的治疗潜力,实现从免疫调控到基因编辑的多层次治疗突破。其次,应推动该平台的临床转化研究,通过扩大动物模型规模、优化给药方案及开展安全性评价,加速其向临床应用迈进。此外,该TBILs设计理念可延伸至其他ROS富集的肿瘤类型(如肝癌、肺癌),验证其跨癌种应用的普适性。最后,通过引入靶向配体或抗体修饰,进一步提升LNPs对PDEC亚群的特异性识别能力,实现真正意义上的细胞精准靶向。总之,这项研究不仅为解决胰腺癌mRNA递送难题提供了创新方案,更为下一代智能纳米药物的开发奠定了坚实基础,有望推动整个核酸药物领域向器官特异性、细胞类型特异性的新时代迈进。
文献信息
X. Qiu, Y. Yang, Q. Ma, et. al., Thioketal-Incorporated Biodegradable Lipid Nanoparticles Deliver mRNA to Ductal Epithelial Cells for Improved Pancreatic Cancer Treatment, J. Am. Chem. Soc., 2025. https://doi.org/10.1021/jacs.5c19387




