
研究背景
肝癌早期诊断与术中微小肿瘤精准定位是提升患者生存率的关键,然而临床仍面临两大核心瓶颈:1.传统荧光成像需实时光激发,易受生物组织自发荧光干扰且穿透深度有限,导致信噪比偏低,难以识别1mm级微小病灶;2.现有分子成像探针大多依赖肿瘤上调生物标志物,而针对肝癌等肿瘤中普遍存在的下调生物标志物的靶向探针十分匮乏,限制了肿瘤与正常组织的精准区分。尽管分子余辉成像因激发停止后仍能持续发光,可有效消除背景荧光、提升成像特异性,被视为极具临床转化潜力的技术,但当前有机余辉探针普遍存在余辉寿命短、需反复现场诱导的问题,无法满足长期纵向监测与术中导航的实际需求。
基于此,南开大学生命科学学院、有机新物质创造前沿科学中心丁丹教授研究团队研发出一款名为DROP的类放射性同位素分子余辉探针。该探针凭借独特的光能量循环机制,实现超40天的超长余辉,且创新性靶向下调的肝癌生物标志物CYP450,在小鼠和兔子模型中精准识别1mm微小肿瘤,为癌症诊断与术中导航提供了全新解决方案。相关内容以“Radioisotope-mimetic molecular afterglow probe for downregulated cancer biomarker imaging”为题发表在《Nature Materials》,南开大学有机新物质创造前沿科学中心为论文通讯单位。
研究内容

图1:DROP的设计理念与类放射性同位素余辉成像原理
图中清晰对比了传统成像与本研究的核心差异:a部分展示传统荧光成像依赖肿瘤上调生物标志物,而DROP通过检测下调生物标志物(如CYP450)实现肿瘤特异性余辉激活——正常肝组织中高表达的下调标志物加速探针代谢,余辉信号关闭,肿瘤组织中标志物下调,余辉信号持续开启;b部分凸显DROP的类放射性优势,传统余辉探针需反复现场诱导(仅维持分钟级成像),而DROP经体外预诱导后,单次注射即可实现8小时以上无诱导纵向成像,规避了光穿透深度不足的问题。

图2:DROP的组成筛选与超长余辉机制
图中系统呈现了探针的优化过程与发光机制:a部分为DROP的组成示意图,包含余辉底物(AS系列)、引发剂(AI系列)及DSPE-PEG₂₀₀₀稳定剂;b、c部分通过筛选实验证实,AS2是最优余辉底物(余辉强度是其他底物的5倍以上),AI2是最优引发剂,二者1:2比例搭配时余辉最强;d部分显示DROP的近红外发射峰位于667nm,适配生物成像需求;e-h部分揭示核心机制:经一次光诱导后,AI2产生¹O₂氧化AS2生成高能中间体AS2-i,AS2-i分解发光并通过ARET重新激发AI2,实现¹O₂与中间体的持续再生,形成自可持续循环,最终达成40天超长余辉。
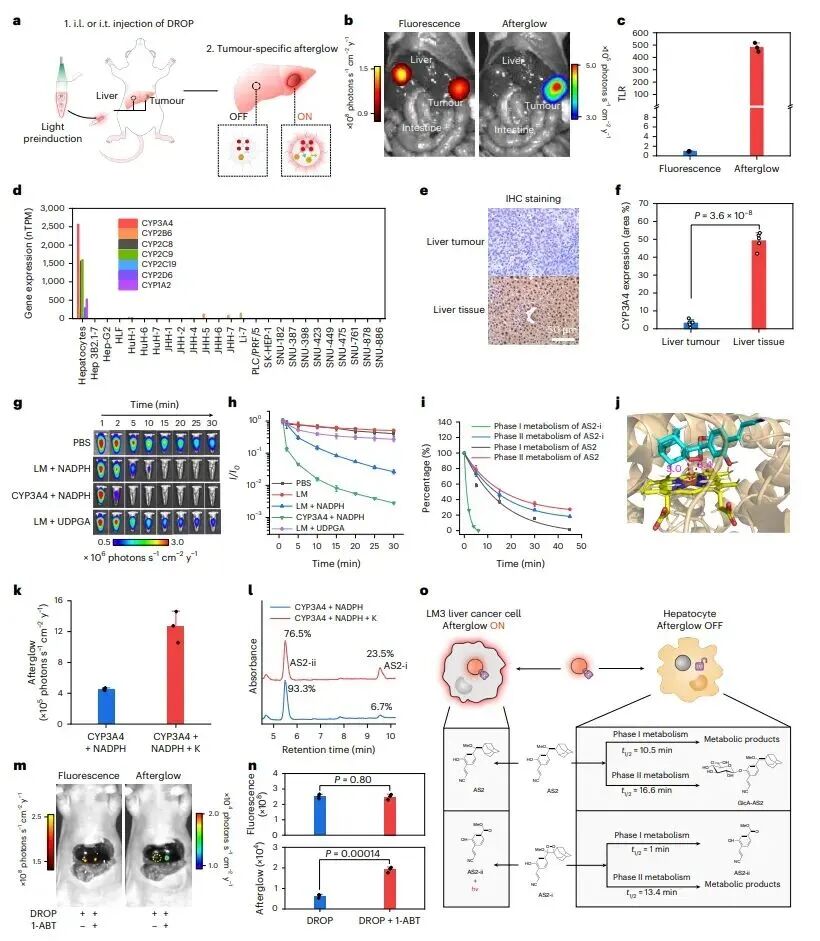
图3:DROP在肝脏中的代谢失活机制
图中阐明了探针肿瘤特异性的分子基础:a-c部分通过局部注射实验证实,DROP在肿瘤组织中产生强余辉信号(SBR=758.6),在正常肝组织中信号微弱(SBR=1.57),肿瘤-肝脏比值(TLR)高达481.3;d-f部分通过数据库分析与免疫组化验证,正常肝细胞中CYP450酶(如CYP3A4)表达量是肿瘤细胞的13.6倍以上;g-l部分通过体外代谢实验证明,CYP450介导的I相代谢可快速降解探针中间体AS2-i(半衰期仅1分钟),而II相代谢作用微弱;m-o部分通过抑制剂实验(CYP3A4抑制剂酮康唑、广谱抑制剂1-ABT)进一步验证,CYP450酶的代谢作用是正常肝组织中探针余辉关闭的关键。

图4:小鼠原位肝癌模型中的成像与术中导航
图中验证了DROP在小鼠模型中的应用价值:a-c部分显示,经静脉注射预诱导DROP后,6小时时肿瘤组织余辉TLR达260.1(SBR=370.9),远优于荧光成像(TLR≈1.5),且在1cm厚肝组织覆盖下仍保持高对比度成像;d-f部分证实,DROP在急性肝损伤、肝纤维化等病理模型中无明显余辉信号,仅在肿瘤组织中激活,具备良好的疾病特异性;g-j部分在PDX模型中,DROP可清晰勾勒1mm微小肿瘤边界,TLR高达274.7,引导手术实现肿瘤完整切除,术后残留余辉信号极低,经组织学验证无肿瘤残留。
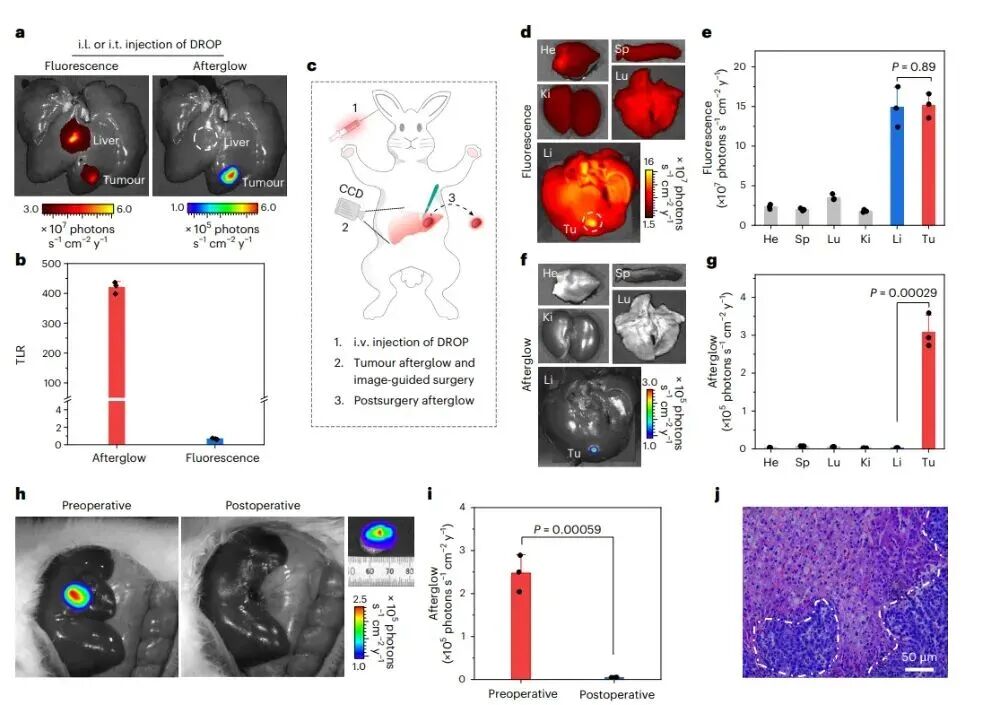
图5:兔子原位肝癌模型中的成像与手术验证
图中进一步验证了DROP的临床转化潜力:a-b部分通过原位注射实验,DROP在兔子肿瘤组织中TLR达420.2,正常肝组织余辉信号被有效抑制;c-g部分显示,静脉注射后1分钟即可实现肿瘤成像,TLR高达2508.6,远优于荧光成像,离体器官成像也证实肿瘤组织特异性富集;h-j部分通过术中导航,成功切除1mm微小肿瘤,术后组织学染色与余辉成像均确认肿瘤完全切除,证明DROP在大动物模型中仍具备高效的成像与导航能力。
全文总结
本研究创新性地开发了一款兼具超长余辉与下调生物标志物靶向性的DROP探针,通过自可持续光能量循环机制,将余辉时长延长至40天,突破了传统探针的时间限制;同时以肿瘤下调的CYP450酶为靶点,实现健康组织与肿瘤组织的精准区分,TLR高达274.7,远超现有成像探针。该探针在小鼠、PDX及兔子模型中均能精准识别1mm微小肝癌,为早期诊断提供可能,且可有效引导肿瘤完整切除,解决了临床中微小肿瘤难以定位的痛点。此外,DROP具备良好的生物相容性与快速体内清除能力,进一步降低了临床应用风险。这项研究不仅为超长余辉探针的设计提供了核心指导原则,更开拓了下调生物标志物在肿瘤诊疗中的应用方向,有望推动光学成像技术从基础研究走向临床转化,为癌症精准医疗带来新的突破。
来源:BioMed科技




