
研究背景
不对称催化的发展始终依赖新型手性催化剂的开发与新反应机理的发现,手性氢键供体(HBD)催化剂因结构多样、功能灵活,被广泛应用于对映选择性 N−H 键插入反应,但其催化效果随底物类型差异显著,酰胺类底物的不对称 N−H 插入反应始终存在挑战,α- 烷基重氮酯与酰胺的反应更是因烷基取代烯醇中间体稳定性低、烷基链柔性阻碍催化剂 - 底物刚性复合物形成,难以实现高效对映控制;同时 DNA 中腺嘌呤 - 胸腺嘧啶碱基对的协同质子转移天然机制为新型 HBD 催化剂设计提供了灵感,而传统脒类衍生物胍因 pKa 值过高仅能作为强碱,无法直接供质子,亟需开发结构适配的脒类催化单元。
研究内容
近日,南开大学化学学院、有机新物质创造前沿科学中心周其林院士团队在JACS期刊上发表了题为“Chiral Isourea-Catalyzed Enantioselective Carbene Insertion into an N−H Bond through a Double Proton-Transfer Process”的论文。南开大学有机新物质创造前沿科学中心为论文通讯单位。
受生物体系质子转移机制启发,设计并合成了一类新型手性异脲氢键供体催化剂,该催化剂整合了可介导质子穿梭的酸性异脲单元、通过共轭效应微调 pKa 的取代芳基以及诱导对映选择性的刚性环状手性骨架,经一锅两步法合成得到系列异脲催化剂并完成筛选,确定异脲 4 为最优催化剂;以该催化剂实现了 α- 烷基重氮酯与酰胺 N−H 键的高对映选择性插入反应,拓展了酰胺和 α- 烷基重氮酯类底物的适用范围,还将该方法成功应用于生物活性分子的后期官能化及药物相关分子的合成;通过位阻、电子效应分析结合密度泛函理论(DFT)计算,揭示了该反应中前所未有的双质子转移反应机理,阐明了催化剂的 pKa 值、位阻效应、非共价相互作用(π-π 堆叠、氢键)在调控反应对映选择性中的核心作用,明确双质子转移机理的能垒远低于传统单质子转移机理,且异脲催化剂可在反应中自再生。
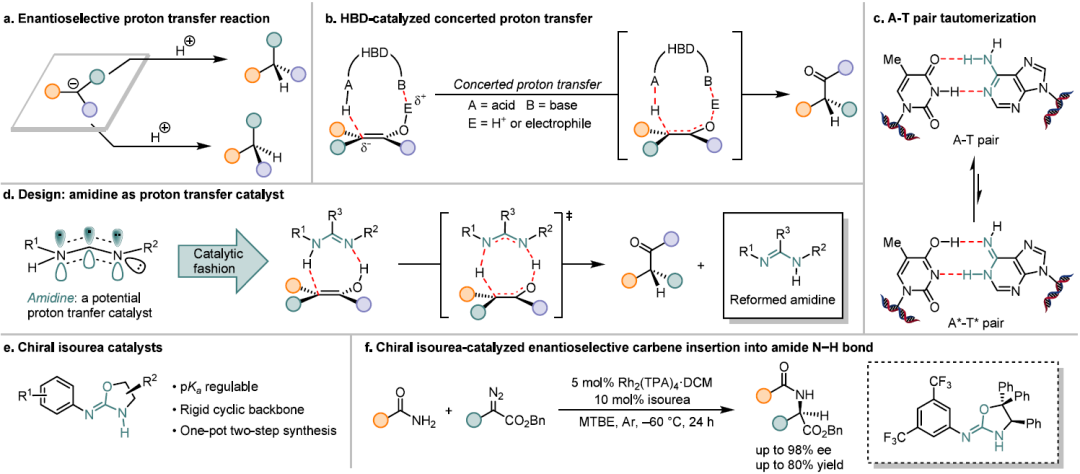
文章亮点
催化剂设计创新
首次开发出以手性异脲为核心的新型 HBD 催化剂,突破了传统脒类衍生物仅能作为强碱的局限,通过结构整合实现了质子供体能力、pKa 值可调、手性诱导的多重功能,且催化剂可在反应中无额外能量输入和步骤的情况下自再生,结构设计兼具创新性与实用性。
发现全新反应机理
通过实验与理论计算结合,揭示了独特的双协同质子转移反应机理,该机理的反应能垒较传统单质子转移机理降低 5.6 kcal/mol,从分子层面阐明了反应高效性的本质,为不对称质子转移反应的机理研究提供了新视角。
结论与展望
该研究成功开发出一类以手性异脲为核心的新型氢键供体催化剂,凭借刚性环状手性骨架、可调控 pKa 的取代芳基与质子穿梭异脲单元的协同结构优势,首次实现 α- 烷基重氮酯与酰胺 N−H 键的高对映选择性插入,攻克了酰胺作为不对称 N−H 插入底物的长期难题,产物 ee 值最高达 98%,且兼容多种官能团。通过实验与 DFT 计算结合,揭示了该反应独特的双质子转移机理,明确催化剂位阻、质子供体能力及底物与催化剂间的 π-π 堆叠、氢键等非共价相互作用是立体控制的核心,该机理能垒更低且催化剂可自再生,为不对称质子转移反应提供了新的机制认知。该方法还成功应用于生物活性分子后期官能化及药物相关分子合成,展现出良好的实际应用价值。未来研究将围绕拓展该手性异脲催化剂的反应适用范围展开,探索其在传统氢键供体催化剂难以实现的不对称转化中的应用;同时将基于现有机理认知,进一步优化催化剂结构,提升其催化效率与底物普适性,推动该类催化剂在更多手性合成领域的产业化应用,为不对称催化的发展提供新的技术与理论支撑。
文献信息
X. Zhang, J. Chen, M. Ye, et. al., Chiral Isourea-Catalyzed Enantioselective Carbene Insertion into an N−H Bond through a Double Proton-Transfer Process, J. Am. Chem. Soc., 2026, doi.org/10.1021/jacs.6c01890.
来源:手性功能材料




