史林启、苏循成、马飞贺:α-突触核蛋白的Tyr39磷酸化加速异质聚集并驱动毒性放大
2026-03-31

引言
近日,南开大学化学学院、有机新物质创造前沿科学中心史林启教授、苏循成教授、马飞贺副教授团队在国际顶尖学术期刊JACS发表题为“Tyr39 Phosphorylation of α-Synuclein Accelerates Heterotypic Aggregation and Drives Toxic Amplification”的研究论文,史林启教授、苏循成教授、马飞贺副教授共同为文章通讯作者,南开大学有机新物质创造前沿科学中心为论文通讯单位。
文章亮点
总结
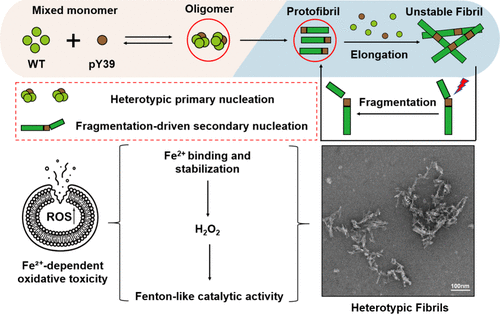
c-Abl介导的α-突触核蛋白Tyr39位磷酸化与帕金森病(PD)的进展高度相关,但Tyr39磷酸化的α-突触核蛋白(pY39-α-syn)在突触核蛋白病中的机制基础仍不清楚。
在此,我们展示了少量的pY39-α-syn显著加速野生型α-突触核蛋白(WT-α-syn)的聚集,并且克服了Hsc70的抑制作用。动力学、连续波电子顺磁共振(EPR)、冷冻透射电子显微镜(cryo-TEM)以及[15N,1H]-NMR谱分析表明,pY39-α-syn参与初级成核,产生异质核,这些核主要通过基于断裂的途径促进二级成核。由此形成的异型聚集体在结构上是不稳定的,形成短的、预先形成的纤维状样组装体,促进α-突触核蛋白种类的毒性放大。
此外,更具毒性的B型寡聚体由这些异型组装体衍生的中间聚集体产生。值得注意的是,我们进一步展示了这些异型聚集体通过结合并稳定Fe2+而具有芬顿样催化活性,为帕金森病进程中Fe2+-依赖的氧化毒性提供了新的机制性见解。
总体而言,这项研究系统阐明了Tyr39磷酸化如何重编程α-突触核蛋白的聚集以促进毒性放大,为与帕金森病相关的α-突触核蛋白病提供了新的见解。
来源:探寻新知




