
研究背景
选择性生物分子修饰在现代生物医学领域具有重要的应用价值。尽管针对硫醇、氨基等高活性官能团的修饰方法已日趋成熟,但复杂多肽与蛋白质中丝氨酸(Ser)、苏氨酸(Thr)的羟基侧链仍是极具挑战性的修饰靶点。Ser与Thr是生物体内关键的功能氨基酸,参与磷酸化、糖基化等重要翻译后修饰,但其羟基固有的低亲核性与弱酸性,致使其在复杂体系中难以实现高效的化学选择性修饰;此外,多肽体系中巯基、氨基等高反应性基团,以及酚羟基、羧酸等含羟基结构的竞争反应位点(图1a),加大了Ser/Thr位点选择性修饰的难度。
此前,董家佳与Sharpless的研究发现,氟磺酰异氰酸酯(FSI,图1c)在乙腈、二氯甲烷等有机溶剂中可与多种醇快速反应,但该反应体系缺乏化学选择性,FSI易与胺、氮杂芳烃、酚类及羧酸发生副反应,无法应用于复杂多肽的羟基特异性修饰。
研究内容
近日,针对这一瓶颈,南开大学化学学院、有机新物质创造前沿科学中心陈弓教授团队结合FSI反应特性、异氰酸酯-醇缩合反应机理,并基于前期课题组在溶剂调控多肽侧链反应性方面的研究基础,发现以六氟异丙醇(HFIP)为反应溶剂,可精准调控FSI的反应活性,在室温条件下1分钟内即可完成多肽、蛋白质中Ser/Thr侧链羟基的快速、高选择性标记。经FSI标记的多肽既能与多种胺类化合物发生分子间SuFEx取代反应,生成磺酰胺偶联产物;也可与赖氨酸侧链发生分子内大环化反应,通过Ser/Thr-Lys位点构建订书肽。值得注意的是,修饰在Ser/Thr上的氟磺酰氨基甲酸酯标签可在碱性水相中简便脱除,生成脱氢氨基酸残基;该中间体可进一步与硫醇、胺、膦等亲核试剂发生一锅Michael加成,以脱氧修饰的方式将多肽的醇羟基侧链转化为杂原子连接型衍生物。
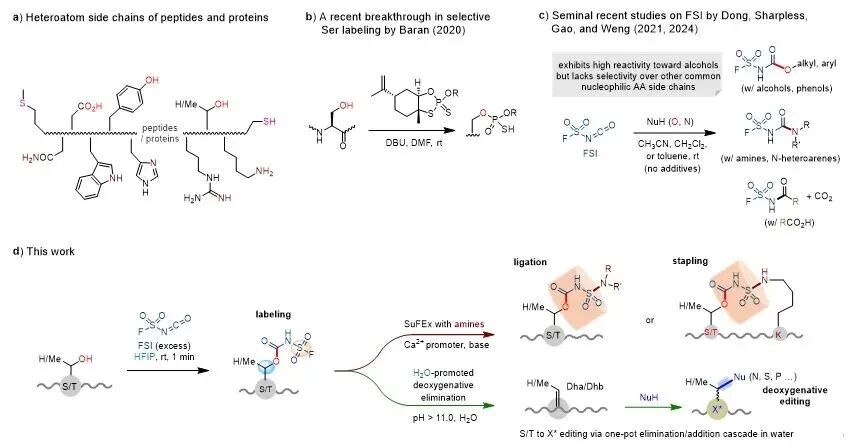
图1. 多肽中醇侧链的选择性标记
如图2所示,作者成功实现了Ser/Thr侧链的快速选择性标记。以同时含Ser与Lys的三肽NA-Ser-Ala-Lys-NH₂(1)为模型,在HFIP中加入8当量FSI,室温反应1.0 min后以甲醇淬灭;LC-MS分析表明,Ser选择性标记的氟磺酰氨基甲酸酯产物1-O产率接近定量转化,且未检测到赖氨酸侧链标记的磺酰脲副产物1-N。将反应时间延长至30 min,仍无O,N 双标记副产物1-ON生成。此外,在三氟乙酸(TFA)溶剂中反应(条件[C]),亦可高选择性、高产率得到1-O。结合实验与密度泛函理论(DFT)计算推测,HFIP溶剂与生成的氟磺酰氨基甲酸酯产物均可作为质子梭,显著提升醇类底物的反应活性。HFIP的选用对实现高化学选择性与高反应活性至关重要:其通过质子化作用有效抑制赖氨酸侧链反应性,在促进丝氨酸修饰的同时,不会大量消耗FSI试剂。
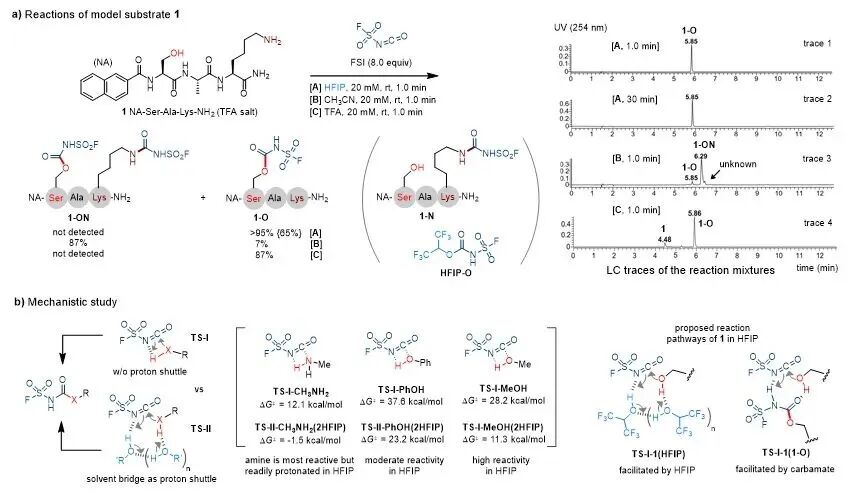
图2. 使用FSI对多肽底物1进行丝氨酸选择性标记的研究
随后,该团队探究了该标记反应的多肽底物适用范围。如图3所示,标准条件下,该丝氨酸标记方法可适用于多种N端保护的多肽底物。除半胱氨酸(Cys)外,其余蛋白源氨基酸在标准条件[A]下均展现出良好的官能团耐受性。环肽药物阿托西班(14)、环肽cyclo (RGDfT)(19)、大环抗生素达托霉素(20)、细胞毒素单甲基奥瑞他汀E(MMAE,18)及环孢菌素A(15)等多种生物活性多肽,均可在丝氨酸/苏氨酸位点实现高选择性标记,且产率优良至优异。
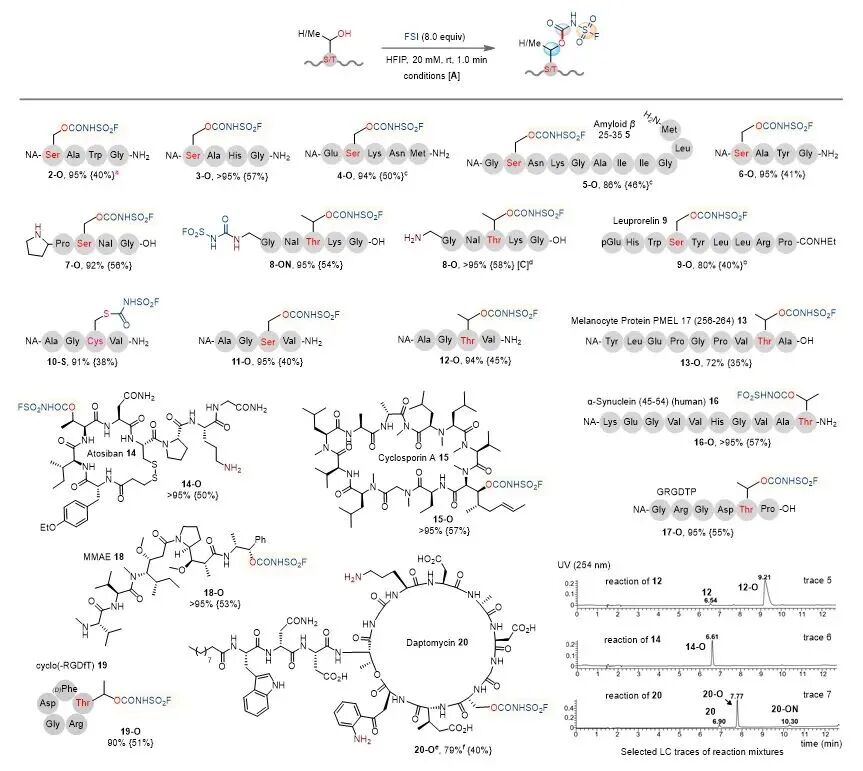
图3. 在HFIP中FSI选择性标记Ser/Thr肽的底物适应范围
接着该团队采用路易斯酸催化剂(Ca(OTf)2/Ca(NTf2)2)与强有机碱1,4-二氮杂双环[2.2.2]辛烷(DABCO)联用体系,在温和条件下实现了FSI标记多肽与胺类的高效SuFEx连接反应(图4)。胺类反应性方面,仲胺活性普遍优于伯胺(比较11-O-22与11-O-23),部分伯胺亦表现良好(如11-O-21)。多种烷基胺(含药物分子阿格列汀24、阿莫沙平25、度洛西汀27)均可与底物11高效偶联,总产率优异;与N-炔基哌嗪衍生物26反应,得到11-O-26,LC产率达92%。芳胺虽活性较低,但仍可参与转化(如11-O-28)。在混合溶剂体系(条件[F])下,帕博西尼29、荧光团30、生物素31等复杂胺类结构,均能以良好产率与复杂多肽底物完成SuFEx连接。
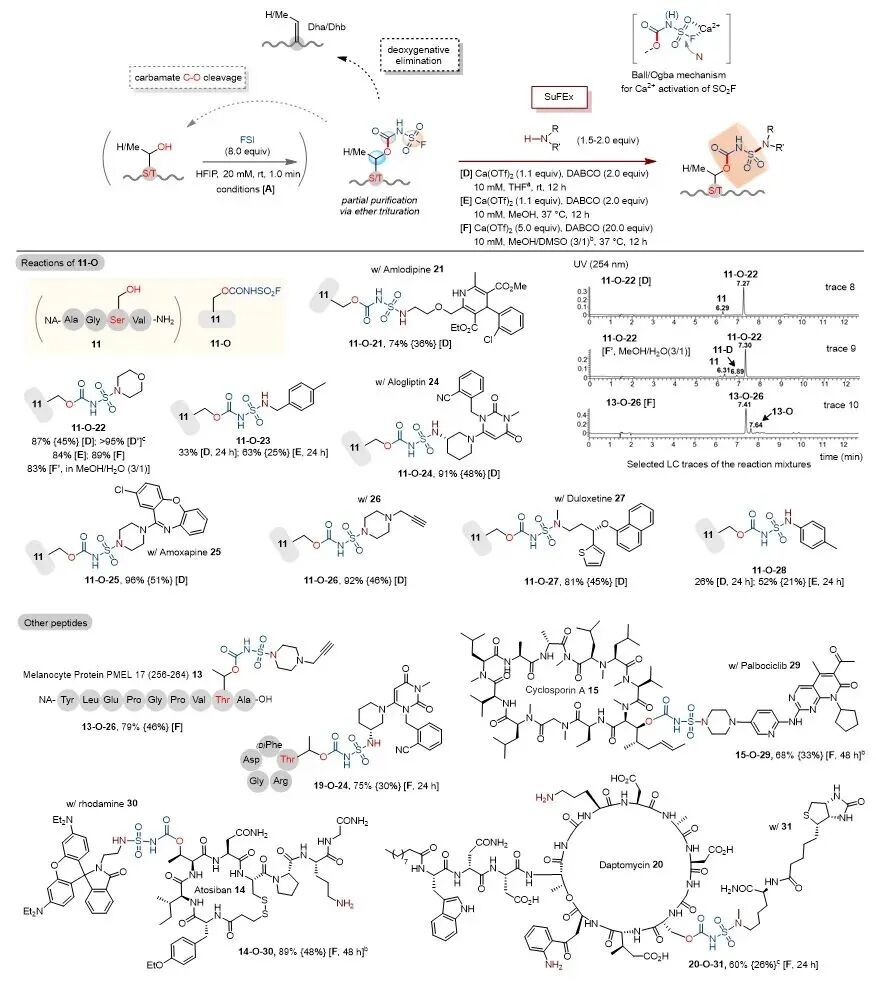
图4. FSI标记的肽与胺的SuFEx偶联
如图5所示,该团队进一步发现,在Ca²⁺/DABCO介导下,氟磺酰氨基甲酸酯基团可与邻近赖氨酸(Lys)的伯胺侧链发生分子内取代反应,由此建立了一种基于醇-胺侧链配对的多肽两步钉合新策略。
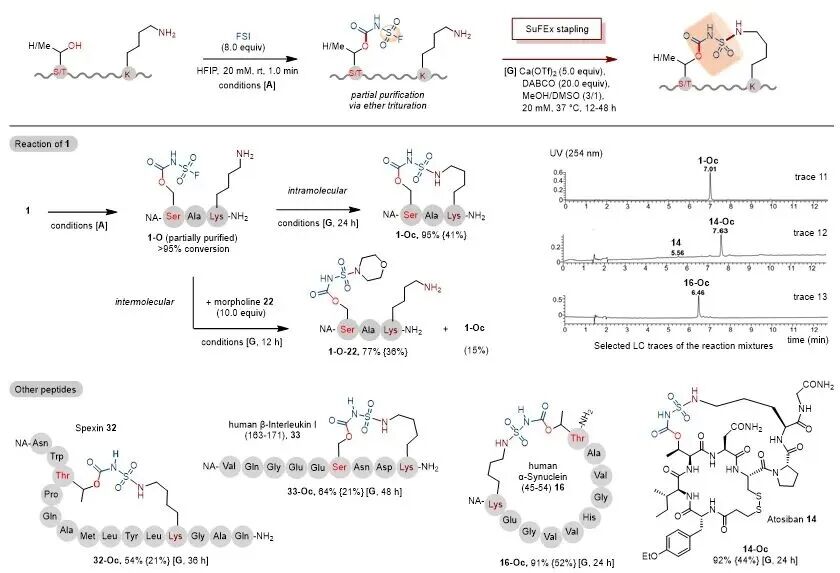
图5. 基于FSI标记与分子内SuFEx取代的Ser/Thr-Lys构建订书肽
该团队在考察11-O稳定性及与胺的SuFEx反应时,意外发现碱性水环境下会生成烯烃消除产物11-D。后续研究证实,丝氨酸衍生的氟磺酰氨基甲酸酯在温和碱性水溶液中可高效发生烯烃消除(图6a)。研究结果表明,小体积、强碱性的氢氧根离子可高效攫取氨基甲酸酯修饰的Ser/Thr残基α-质子,触发消除形成烯烃;而大位阻有机碱(如DIPEA、NEt₃)攫取α-质子效率偏低,在大分子量多肽底物中尤为显著。结合实验与DFT计算结果(图6b),该消除过程更倾向于遵循OH⁻介导、水辅助的协同E2机理,反应能垒较低(ΔG⧧=24.7 kcal/mol);但由于直接去质子化步骤的能垒与之相近(ΔG⧧=23.9 kcal/mol),现阶段尚不能排除反应经由瞬态中间体以分步E1cb机理进行的可能。此外,所生成的脱氢氨基酸残基(Dha/Dhb)可作为多肽通用亲电位点,与硫醇、胺、膦等试剂经一锅法Michael加成,构建多种含杂原子连接的脱氧多肽修饰类似物。
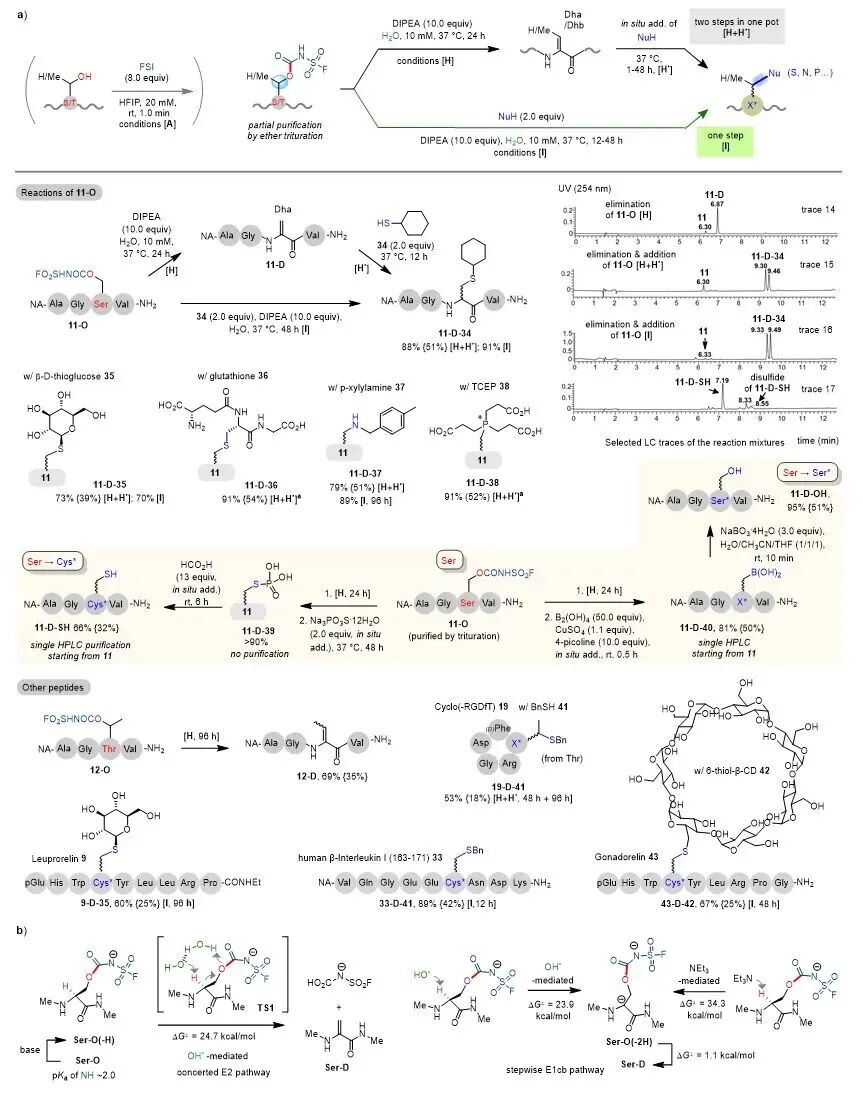
图6. 通过消除-迈克尔加成级联反应对Ser/Thr进行一锅脱氧编辑
如图7所示,经条件优化后,FSI介导的Ser/Thr选择性标记策略可高效应用于蛋白质修饰。以溶菌酶(44)为底物,反应生成最多携带9个氨基甲酸酯标签的偶联物44-On;胰蛋白酶酶解片段的串联质谱(MS-MS)分析证实,其17个Ser/Thr残基中16个被特异性标记,且无非目标位点修饰。圆二色谱(CD)表征显示,标记后溶菌酶的二级结构与天然酶基本保持一致。同理,核糖核酸酶A(45)经标记后得到产物45-On,最多可引入7个氨基甲酸酯标签。
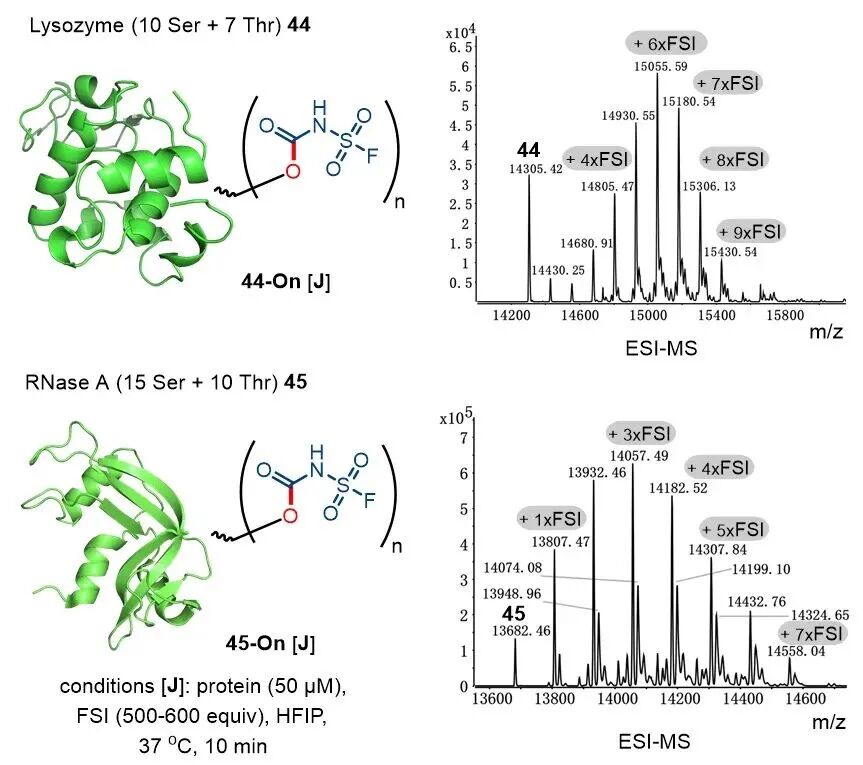
图7. 在HFIP中利用FSI实现蛋白质的Ser/Thr选择性标记
综上,陈弓教授团队建立了一种以FSI为双亲电试剂、以HFIP为反应介质的选择性标记体系,实现了从多肽Ser/Thr羟基侧链到氟磺酰氨基甲酸酯中间体的快速转化(室温、1 min)。该标记并非终点,而是一个可编程节点。所得FSI标记产物,既可通过SuFEx反应与胺类化合物偶联,生成稳定的磺酰胺偶连产物;也可与邻近赖氨酸侧链发生分子内大环化反应。此外,在碱性水相中,该标签可发生选择性消除生成脱氢氨基酸(Dha/Dhb),作为亲电中心进一步与硫醇、胺、膦等试剂发生一锅Michael加成,实现“脱氧编辑”。该体系为长期难以实现选择性修饰的多肽Ser/Thr羟基侧链,提供了一套简便高效的位点选择性编辑新策略。
相关工作最近发表在J. Am. Chem. Soc.上。南开大学化学学院、有机新物质创造前沿科学中心陈弓教授、初鑫博士和山东大学陆刚教授为共同通讯作者,南开大学博士研究生张董为该论文的第一作者,山东大学陆刚课题组对反应机理计算部分提供了重要支持,南开大学硕士研究生苗新涛对该工作的顺利进行也做出了重要贡献,南开大学有机新物质创造前沿科学中心为论文通讯单位。
文献信息
Fast and Selective Labeling of Serine and Threonine in HFIP for Facile Editing of Peptide Alcohol Side Chains, Dong Zhang, Limeng Wang, Xintao Miao, Shuai Jiang, Xiaowei Sun, Xiaoxi Xu, Jiajia Dong, Gang Lu*, Xin Chu*, Gong Chen*, J. Am. Chem. Soc. 2026, DOI: 10.1021/jacs.6c04665
来源:X-MOL资讯




